
15/12/2024 12:05
Công thức hóa học của rượu etylic trong cuộc sống

1. Công thức hóa học của rượu
Rượu, đặc biệt là rượu etylic (ethanol), là một trong những hợp chất hữu cơ nổi bật trong cuộc sống hàng ngày của chúng ta. Rượu không chỉ có mặt trong các món đồ uống có cồn như bia, rượu vang mà còn được ứng dụng rộng rãi trong nhiều lĩnh vực khác nhau, từ dược phẩm đến công nghiệp.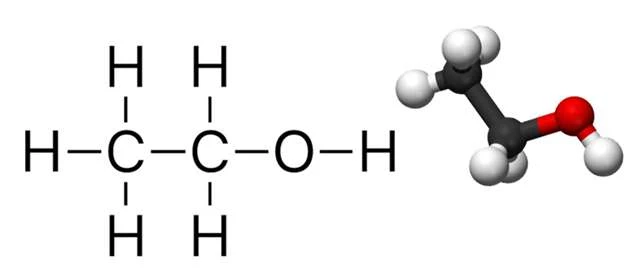
Công thức và cấu trúc của rượu etylic
- Công thức chung: C2H6O
- Công thức hóa học: C2H5OH
- Công thức phân tử: CH3-CH2-OH
- Khối lượng phân tử: 46 g/mol
2. Tính chất hóa học của rượu etylic
Rượu etylic là một đại diện đặc trưng cho các ancol mà trong đó có một nhóm hydroxyl. Với cấu trúc đơn giản này, rượu etylic thể hiện nhiều tính chất hóa học đáng chú ý.
2.1. Phản ứng với kim loại mạnh
Khi phản ứng với các kim loại mạnh như natri (Na), rượu etylic sẽ tạo ra khí hydro. Quá trình này phản ánh tính chất hóa học của rượu như một acid yếu. Phương trình phản ứng: \[ 2C2H5OH + 2Na \rightarrow 2C2H5ONa + H2\uparrow \]2.2. Phản ứng oxi hóa
Rượu etylic có khả năng dễ cháy cao, khi cháy hoàn toàn, chúng tạo ra nước và khí carbon dioxide mà không phát sinh khói. Phương trình phản ứng cháy: \[ C2H5OH + 3O2 \rightarrow 2CO2 + 3H2O \]2.3. Phản ứng với axit axetic
Khi rượu etylic phối hợp với axit axetic dưới tác dụng của nhiệt và môi trường acid, phản ứng este hóa xảy ra tạo thành este và nước. Phương trình phản ứng: \[ C2H5OH + CH3COOH \rightleftharpoons CH3COOC2H5 + H2O \]3. Tính chất vật lý của rượu
Rượu etylic thể hiện nhiều tính chất vật lý quan trọng:- Hình dáng và mùi: Chất lỏng không màu, trong suốt, có mùi thơm nhẹ và vị cay nồng.
- Khối lượng riêng: 0.789 g/cm³.
- Nhiệt độ sôi: 78.39 độ C.
- Nhiệt độ nóng chảy: 114.15 độ C.
4. Các phương pháp điều chế ancol etylic
Việc điều chế rượu etylic có rất nhiều phương pháp, cả tự nhiên lẫn công nghiệp.4.1. Lên men đường hoặc tinh bột
- Phương pháp: Sử dụng các vi sinh vật, chủ yếu là men để lên men đường hoặc tinh bột.
- Cách thực hiện: Cho đường hoặc tinh bột vào nước, sau đó thêm men để kích thích quá trình lên men.
4.2. Công nghệ Hydrat hóa Etylen
- Phương pháp: Etylen được cho phản ứng với nước có xúc tác.
4.3. Thủy phân dẫn xuất của este
Rượu etylic cũng có thể được tạo ra thông qua các phản ứng thủy phân, ví dụ như thủy phân este: Phương trình phản ứng: \[ C2H5COO-Na + H2O \rightarrow C2H5OH + NaOH \]5. Công thức tính độ rượu
Độ rượu là một chỉ số quan trọng khi nói đến các đồ uống có cồn.- Định nghĩa: Độ rượu cho biết tỷ lệ phần trăm thể tích ethanol nguyên chất có trong 100ml dung dịch.
- Ví dụ: Rượu 31 độ có nghĩa là trong 100ml rượu có 31ml ethanol.
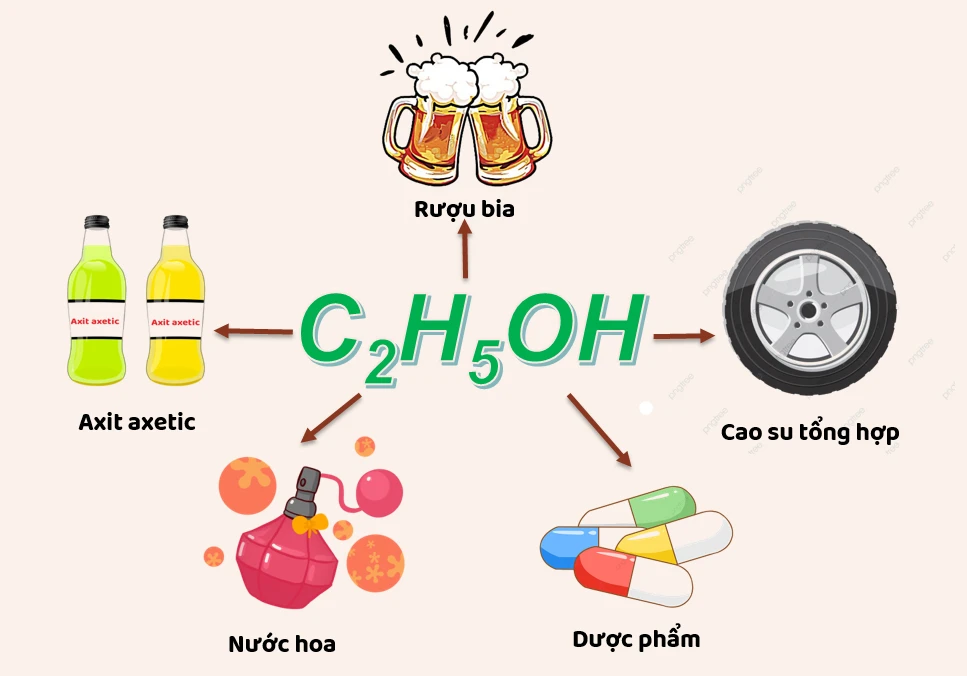
6. Ứng dụng của rượu etylic
Rượu etylic có rất nhiều ứng dụng trong cuộc sống và trong công nghiệp, bao gồm:- Sản xuất dược phẩm và đồ uống có cồn: Nguyên liệu chính trong sản xuất rượu và bia.
- Dung môi: Sử dụng để pha chế vecni, nước hoa và các sản phẩm hóa học.
- Nhiên liệu cồn: Được sử dụng như một nguồn nhiên liệu xanh, thường được pha trộn với xăng.
- Khử trùng và tẩy uế: Dung dịch chứa 70% etanol rất hiệu quả trong việc tiêu diệt vi khuẩn và virus.
Tác hại của rượu etylic
Mặc dù rượu etylic có nhiều công dụng tích cực, nhưng việc tiêu thụ quá mức có thể gây hại nghiêm trọng cho sức khỏe, ảnh hưởng đến khả năng kiểm soát hành vi và có thể dẫn đến các tai nạn ngoài mong muốn.Kết luận
Rượu etylic không chỉ là một hợp chất hóa học đơn giản mà còn mang lại nhiều giá trị thiết thực cho xã hội. Hiểu rõ về công thức, tính chất và ứng dụng của rượu sẽ giúp chúng ta có cái nhìn toàn diện hơn về chất này trong đời sống hàng ngày. Hãy sử dụng một cách hợp lý và có trách nhiệm để bảo vệ sức khỏe cho chính mình và cộng đồng. Để mở rộng kiến thức của bạn về rượu etylic và các hợp chất hóa học khác, hãy tiếp tục theo dõi các bài viết chuyên sâu trên trang Vuihoc.vn!
Link nội dung: https://bitly.vn/cong-thuc-hoa-hoc-cua-ruou-etylic-trong-cuoc-song-a15866.html