
15/12/2024 14:40
Dãy hoạt động hóa học của kim loại và ứng dụng thực tiễn
Dãy Hoạt Động Hóa Học Của Kim Loại Là Gì?
Dãy hoạt động hóa học của kim loại là một khái niệm quan trọng trong hóa học, thể hiện khả năng tham gia phản ứng hóa học của các kim loại. Các kim loại được sắp xếp theo thứ tự từ có tính hoạt động cao đến thấp, giúp học sinh dễ dàng dự đoán các phản ứng hóa học có thể xảy ra.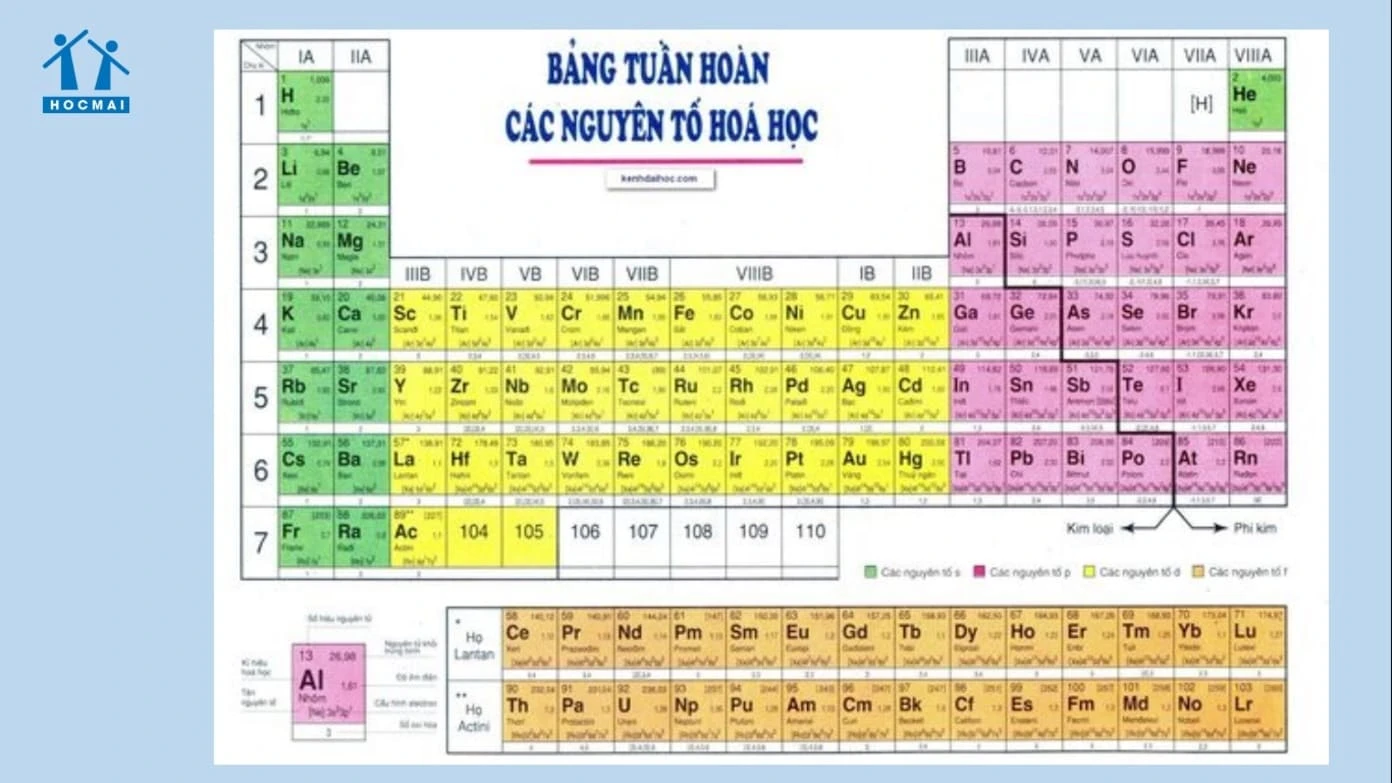
Phiên Bản Ngắn Gọn Dãy Hoạt Động Hóa Học
- K, Na, Ca, Mg, Al, Zn, Fe, Ni, Sn, Pb, (H), Cu, Hg, Ag, Pt, Au

Phiên Bản Đầy Đủ Dãy Hoạt Động Hóa Học
- Li, K, Sr, Ca, Na, Mg, Al, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, (H), Sb, As, Bi, Cu, Hg, Ag, Pd, Pt, Au

Mẹo Học Thuộc Lòng Dãy Hoạt Động Hóa Học Kim Loại
Để ghi nhớ dãy hoạt động hóa học một cách dễ dàng, bạn có thể áp dụng một câu thần chú đơn giản. Câu này không chỉ giúp bạn ghi nhớ dễ dàng mà còn tạo ấn tượng thú vị, đó là:"Khi nào áo giáp sắt nhớ sang phố hỏi cửa hàng Á Phi Âu."
Cách Học Tốt Hóa Học
Dưới đây là 5 bước giúp bạn học tốt môn Hóa học:- Chú Ý Đến Tính Chất Của Kim Loại: Nắm rõ sự khác biệt giữa các nhóm kim loại trong dãy hoạt động.
- Thực Hành Thường Xuyên: Làm nhiều bài tập liên quan đến phản ứng giữa kim loại và axit, muối.
- Sử Dụng Ảnh Hưởng Thực Tế: Tìm hiểu cách mà dãy hoạt động ảnh hưởng đến các lĩnh vực công nghiệp và đời sống.
- Ghi Nhớ Qua Trò Chơi: Sử dụng ứng dụng học tập để chơi trò chơi liên quan đến hóa học.
- Tham Gia Nhóm Học: Học cùng bạn bè để cùng nhau khám phá và trao đổi kiến thức.
Tính Chất Của Dãy Hoạt Động Hóa Học Kim Loại
1. Mức Độ Hoạt Động Hóa Học Của Kim Loại Giảm Từ Trái Sang Phải
- Kim loại K (Kali) là kim loại mạnh nhất.
- Kim loại Au (Vàng) là kim loại yếu nhất.
- Nhóm kim loại mạnh: Li, K, Ba, Ca, Na.
- Nhóm kim loại mạnh: Mg, Al.
- Nhóm kim loại trung bình: Mn, Zn, Cr, Fe, Ni, Sn, Pb.
- Nhóm kim loại yếu: Cu, Hg, Ag, Pt, Au.
2. Phản Ứng Các Kim Loại Với Nước
Chỉ những kim loại đứng trước Mg mới có thể phản ứng với nước ở nhiệt độ thường. Ví dụ:- Na + H₂O → NaOH + H₂
3. Phản Ứng Với Dung Dịch Axit
Các kim loại đứng trước H có khả năng phản ứng với dung dịch axit mạnh, tạo ra khí H₂. Ví dụ:- Fe + 2HCl → FeCl₂ + H₂
- Cu + 2HCl → không có phản ứng (vì Cu đứng sau H).
4. Đẩy Kim Loại Khác Khỏi Dung Dịch Muối
Kim loại không tan trong H₂O có thể đẩy được chất đứng sau nó khỏi dung dịch muối. Ví dụ:- Fe + CuSO₄ → FeSO₄ + Cu
- Cu + 2AgNO₃ → Cu(NO₃)₂ + 2Ag
Bài Tập Vận Dụng Dãy Hoạt Động Hóa Học Hóa 9
Để củng cố kiến thức, dưới đây là một số bài tập vận dụng dãy hoạt động hóa học dành cho học sinh lớp 9:Câu 1: Sắp Xếp Theo Chiều Tăng Dần
Dưới đây là một vài dãy kim loại, bạn hãy cho biết dãy nào được sắp xếp theo chiều tăng dần của dãy hoạt động hóa học:- Mg, Al, Ni, Sn, Au
- K, Ba, Na, Au, Fe
- Fe, Cu, K, Mg, Al, Zn
- Mg, K, Cu, Al, Fe
Câu 2: Thí Nghiệm Tạo Khí
Bạn An đã thực hiện các thí nghiệm sau, hãy cho biết thí nghiệm nào tạo khí:- a) Cho mẩu Natri vào nước.
- b) Nhúng thanh nhôm vào bể nước.
- c) Cho bột nhôm vào nước.
- d) Cho dung dịch kiềm của Natri vào nước.
Câu 3: Tính Toán Hóa Học
Cho 21 gam hỗn hợp 2 kim loại Cu, Zn vào dung dịch H₂SO₄ loãng dư, thu được 4,48 lít khí (đktc). a. Viết phương trình phản ứng hóa học. b. Tính khối lượng chất rắn còn lại sau phản ứng. Lời giải:- Phương trình hóa học:
- Khối lượng của kẽm:
- Khối lượng của đồng:
Tài Nguyên Hỗ Trợ
Nếu bạn cần thêm đề kiểm tra Hóa học MIỄN PHÍ với đáp án chi tiết và hướng dẫn giải, hãy khám phá ngay App HOCMAI - ứng dụng học online hàng đầu dành cho học sinh Việt Nam. Bạn sẽ có cơ hội học tập cùng giáo viên danh tiếng, thi thử với kho đề “siêu khủng” và nhận hỗ trợ tư vấn 24/7.Kết Luận
Dãy hoạt động hóa học của kim loại không chỉ là kiến thức cơ bản mà còn là chìa khóa giúp bạn hiểu rõ hơn về hóa học. Hy vọng rằng qua bài viết này, bạn đã nắm vững lý thuyết và áp dụng hiệu quả trong các bài tập. Chúc bạn học tốt môn Hóa và luôn duy trì niềm đam mê với khoa học!
Link nội dung: https://bitly.vn/day-hoat-dong-hoa-hoc-cua-kim-loai-va-ung-dung-thuc-tien-a15882.html