Giới thiệu về bảng tuần hoàn hóa học lớp 7
Bảng tuần hoàn hóa học là một công cụ cực kỳ quan trọng trong môn hóa học, không chỉ giúp chúng ta hiểu rõ về các nguyên tố hóa học mà còn cung cấp thông tin cần thiết về tính chất và mối quan hệ giữa chúng. Trong bài viết này, chúng ta sẽ cùng nhau tìm hiểu về lý thuyết cơ bản của bảng tuần hoàn hóa học lớp 7, cùng những nguyên tắc, cấu tạo và phân loại các nguyên tố hóa học.

I. Nguyên Tắc Sắp Xếp Các Nguyên Tố Hóa Học Trong Bảng Tuần Hoàn

1. Lịch sử hình thành
Bảng tuần hoàn hóa học được xây dựng lần đầu tiên vào năm 1869 bởi nhà bác học người Nga Dmitri Ivanovich Mendeleev. Ông đã tổ chức các nguyên tố hóa học theo chiều tăng dần của khối lượng nguyên tử. Tuy nhiên, với sự phát triển của khoa học, các nhà nghiên cứu hiện đại đã chỉ ra rằng điện tích hạt nhân mới là tiêu chí chính để sắp xếp các nguyên tố.
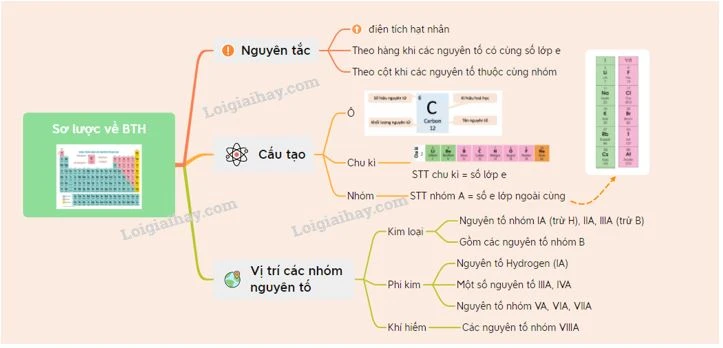
2. Nguyên tắc hiện đại
Hiện nay, bảng tuần hoàn hóa học bao gồm 118 nguyên tố, và được sắp xếp theo các nguyên tắc sau:
- Điện tích hạt nhân: Các nguyên tố hóa học được sắp xếp theo chiều tăng dần của điện tích hạt nhân.
- Số lớp electron: Các nguyên tố trong cùng một hàng (chu kỳ) có cùng số lớp electron trong nguyên tử.
- Tính chất hóa học: Các nguyên tố trong cùng một cột (nhóm) có tính chất hóa học gần giống nhau.

II. Cấu Tạo Bảng Tuần Hoàn Các Nguyên Tố Hóa Học
Bảng tuần hoàn được chia thành các phần chính, mỗi phần có chức năng và ý nghĩa riêng.
1. Ô nguyên tố
Mỗi nguyên tố hóa học được đại diện bởi một ô trong bảng tuần hoàn, gọi là ô nguyên tố. Một ô nguyên tố thường chứa các thông tin sau:
- Số hiệu nguyên tử (Z): Số đơn vị điện tích hạt nhân, bằng số electron trong nguyên tử và là số thứ tự của nguyên tố trong bảng.
- Ký hiệu hóa học: Một hoặc hai chữ cái đại diện cho nguyên tố (ví dụ: H cho Hydro, O cho Oxy).
- Tên nguyên tố: Tên gọi chính thức của nguyên tố.
- Khối lượng nguyên tử: Khối lượng của nguyên tử tính bằng đơn vị khối lượng nguyên tử (u).
2. Chu kỳ
Định nghĩa
Chu kỳ là tập hợp các nguyên tố mà nguyên tử của chúng có cùng số lớp electron. Bảng tuần hoàn hiện nay có 7 chu kỳ, được đánh số từ 1 đến 7.
Phân loại chu kỳ
- Chu kỳ nhỏ: Chu kỳ 1, 2, 3.
- Chu kỳ lớn: Chu kỳ 4, 5, 6, 7.
Ví dụ:
- Chu kỳ 1 gồm hai nguyên tố: H (Hydro) và He (Hélium).
- Chu kỳ 2 gồm 8 nguyên tố từ Li (Lithium) đến Ne (Neon).
- Chu kỳ 3 cũng có 8 nguyên tố từ Na (Natri) đến Ar (Argon).
3. Nhóm
Định nghĩa
Nhóm là tập hợp các nguyên tố có tính chất hóa học tương tự nhau, được sắp xếp theo cột trong bảng tuần hoàn. Bảng tuần hoàn có 8 nhóm A và 8 nhóm B.
Đặc điểm của các nhóm
- Các nguyên tố trong cùng một nhóm A có số electron ở lớp ngoài cùng giống nhau, dẫn đến tính chất hóa học tương tự.
- Khi đi từ trên xuống dưới trong cùng một nhóm, điện tích hạt nhân tăng dần.
- Số thứ tự của nhóm A bằng số electron lớp ngoài cùng trong nguyên tử của nguyên tố thuộc nhóm đó.
III. Vị Trí Các Nhóm Nguyên Tố Kim Loại, Phi Kim Và Khí Hiếm Trong Bảng Tuần Hoàn
1. Các nguyên tố kim loại
Đặc điểm
Trong số 118 nguyên tố hóa học đã biết, có hơn 90 nguyên tố là kim loại. Chúng thường có tính dẫn điện và nhiệt tốt, dễ dàng tạo thành hợp chất với các nguyên tố khác.
Vị trí trong bảng tuần hoàn
- Hầu hết các nguyên tố thuộc nhóm IA, IIA, IIIA và một số nguyên tố ở các nhóm IVA, VA, VIA.
- Các nguyên tố thuộc nhóm IB đến VIIIB, cùng với các nguyên tố lanthanide và actinide ở cuối bảng tuần hoàn.
2. Các nguyên tố phi kim
Đặc điểm
Phi kim thường có tính chất ngược lại với kim loại. Chúng có thể ở thể rắn, lỏng hoặc khí ở điều kiện thường và thường không dẫn điện.
Vị trí trong bảng tuần hoàn
- Hầu hết các nguyên tố thuộc nhóm VA, VIA, VIIA.
- Một số nguyên tố thuộc nhóm IIIA, IVA.
- Nguyên tố H nằm ở nhóm IA.
3. Các nguyên tố khí hiếm
Đặc điểm
Khí hiếm (hay khí quý) bao gồm 7 nguyên tố, có đặc điểm là nguyên tử có lớp electron ngoài cùng bền vững, nên chúng rất ít tham gia vào các phản ứng hóa học.
Vị trí trong bảng tuần hoàn
- Các nguyên tố khí hiếm nằm ở nhóm VIIIA trong bảng tuần hoàn.
IV. Tầm Quan Trọng Của Bảng Tuần Hoàn Hóa Học
Bảng tuần hoàn hóa học không chỉ cung cấp cho chúng ta những kiến thức cơ bản về các nguyên tố mà còn là nền tảng cho việc nghiên cứu và phát triển khoa học hóa học. Nó giúp học sinh và sinh viên dễ dàng tìm ra thông tin về các nguyên tố, từ đó áp dụng vào thực tiễn cuộc sống và nghiên cứu.
Lợi ích trong học tập
- Hỗ trợ trong việc học tập: Bảng tuần hoàn giúp ghi nhớ nhanh chóng các thông tin về nguyên tố.
- Ứng dụng thực tiễn: Kiến thức từ bảng tuần hoàn có thể được áp dụng trong nhiều lĩnh vực như y học, hóa học, công nghệ và nhiều ngành khoa học khác.
Kết luận
Bảng tuần hoàn hóa học lớp 7 là một phần không thể thiếu trong chương trình học, mở ra cánh cửa cho những hiểu biết sâu rộng hơn về thế giới hóa học. Hy vọng qua bài viết này, các bạn sẽ có cái nhìn tổng quát và rõ ràng hơn về bảng tuần hoàn, cũng như tầm quan trọng của nó trong đời sống và khoa học.
Với những kiến thức đã học, hãy tiếp tục khám phá và nghiên cứu thêm về các nguyên tố hóa học để hiểu rõ hơn về thế giới xung quanh bạn!