Giới Thiệu
Trong chương trình Hóa học lớp 9, bài 4 không chỉ là một phần kiến thức cơ bản mà còn mang đến cho học sinh nhiều thông tin hữu ích về các loại axit quan trọng trong thực tiễn. Axit chloride, axit sunfuric, và những tính chất hóa học của chúng là những điểm nhấn chính trong bài học này. Cùng khám phá sâu hơn về các tính chất, ứng dụng và phản ứng hóa học liên quan đến những axit này.
---
1. Tính Chất Hóa Học của Axit HCl
1.1 Tính Chất Hóa Học
Axit Hydrochloric (HCl) là một loại axit mạnh, có những tính chất hóa học đáng chú ý như:
- Độ pH: Axit HCl có thể làm quỳ tím chuyển sang màu đỏ, chứng tỏ tính axit mạnh.
- Phản Ứng với Kim Loại:
- Phương trình phản ứng:
- 2Al (r) + 6HCl (dd) → 2 AlCl3 (dd) + 3H2 (k)
- Phương trình phản ứng:
- Cu(OH)2(r) + 2HCl(dd) → CuCl2(dd) + 2H2O(l)
- Phương trình phản ứng:
- CuO(r) + 2HCl(dd) → CuCl2(dd) + H2O
- Phản Ứng với Muối: (sẽ được tìm hiểu trong bài 9)
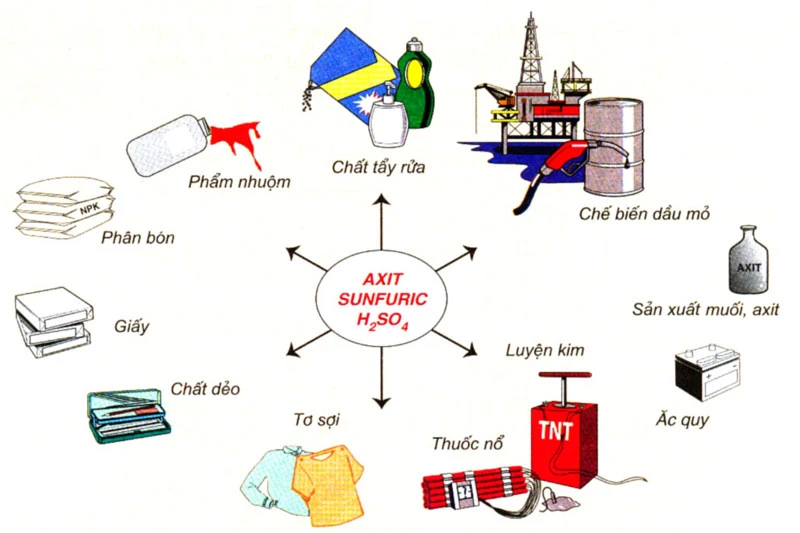
1.2 Ứng Dụng
Axit HCl không chỉ là một chất lý thuyết, mà còn có nhiều ứng dụng trong cuộc sống như:
- Điều Chế Các Muối: Axit HCl được sử dụng rộng rãi để điều chế các loại muối khác nhau.
- Làm Sạch Bề Mặt Kim Loại: Trước khi hàn, HCl được dùng để làm sạch bề mặt kim loại nhằm đảm bảo chất lượng hàn.
- Tẩy Gỉ Kim Loại: Axit HCl là một trong những hóa chất chính được dùng để tẩy gỉ trước khi sơn hoặc mạ kim loại.
- Chế Biến Thực Phẩm và Dược Phẩm: Các ngành thực phẩm và dược phẩm cũng sử dụng HCl để sản xuất và tinh chế sản phẩm.
---
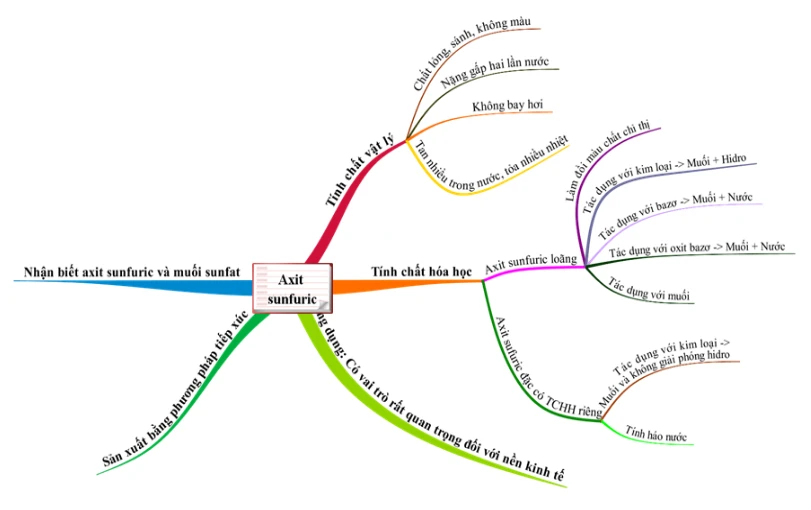
2. Tính Chất Vật Lý và Hóa Học của Axit Sunfuric (H2SO4)
2.1 Tính Chất Vật Lý
H2SO4 là một loại axit không màu, sánh, và có một số tính chất vật lý đáng chú ý:
- Mật Độ: Nặng gấp đôi nước, H2SO4 không dễ bay hơi.
- Độ Tan: Dễ tan trong nước và tỏa nhiều nhiệt khi hòa tan.
Lưu ý: Khi pha H2SO4 loãng, cần cho từ từ axit vào nước, không nên làm ngược lại để tránh nguy hiểm.
2.2 Tính Chất Hóa Học
2.2.1 Axit Sunfuric Loãng (H2SO4l)
- Làm Quỳ Tím Hoá Đỏ: Chứng tỏ tính axit mạnh của H2SO4.
- Tác Dụng với Kim Loại:
- Ví dụ: Mg + H2SO4l → MgSO4 + H2
- Hiện tượng: Xuất hiện khí không màu.
- Ví dụ: H2SO4l + Cu(OH)2 → CuSO4 + 2H2O
- Hiện tượng: Cu(OH)2 tan dần và dung dịch màu xanh xuất hiện.
- Ví dụ: 3H2SO4l + Fe2O3 → Fe2(SO4)3 + 3H2O
- Hiện tượng: Bột Fe2O3 tan dần, tạo dung dịch màu nâu.
- Tác Dụng với Muối: (sẽ được đề cập ở phần sau)
2.2.2 Axit Sunfuric Đặc (H2SO4đ)
- Phản ứng với Đồng:
- Cu + 2H2SO4 (đ) → CuSO4 + SO2 + 2H2O
- Hiện tượng: Khí không màu và dung dịch màu xanh lam.
- Khi cho đường vào H2SO4đ, hình thành khí CO2 và tạo ra carbon đen do phản ứng mạnh mẽ với tính háo nước của axit.
---
3. Quy Trình Sản Xuất Axit Sunfuric
3.1 Nguyên Liệu sản xuất
Axit sunfuric được sản xuất chủ yếu từ lưu huỳnh hoặc quặng pyritsắt (FeS2) theo quy trình tiếp xúc.
3.2 Các Công Đoạn Chính
- Sản Xuất Lưu Huỳnh Đioxit:
- Phương trình phản ứng:
- S + O2 → SO2
- hoặc: 4FeS2 + 11O2 → 2Fe2O3 + 8SO2
- Sản Xuất Lưu Huỳnh Trioxit:
- Phương trình phản ứng:
- 2SO2 + O2 → 2SO3
- Phương trình phản ứng:
- SO3 + H2O → H2SO4
---
4. Kết Tủa BaSO4 và Thí Nghiệm Nhận Biết
4.1 Nhận Biết Gốc Sunfat
- Dung dịch BaCl2, Ba(NO3)2, và Ba(OH)2 được dùng làm thuốc thử để nhận ra gốc sunfat.
4.2 Thí Nghiệm
- Khi kết hợp dung dịch H2SO4 với BaCl2, sẽ xuất hiện kết tủa trắng BaSO4:
- Phương trình hóa học: H2SO4 + BaCl2 → BaSO4 (kết tủa trắng) + 2HCl
---
5. Kết Luận
Bài học về các axit, đặc biệt là axit HCl và H2SO4, không chỉ giúp học sinh nắm vững kiến thức hóa học mà còn cung cấp thông tin ứng dụng thực tiễn trong cuộc sống. Qua đó, chúng ta nhận ra rằng hóa học không chỉ là một môn học, mà còn là nền tảng cho nhiều công nghệ và quy trình trong sản xuất, chế biến thực phẩm, cũng như trong lĩnh vực dược phẩm.
Những kiến thức này sẽ là hành trang quý báu cho học sinh trong tương lai, không chỉ trong việc hiểu biết về khoa học tự nhiên mà còn trong việc ứng dụng vào thực tiễn cuộc sống hàng ngày. Việc nghiên cứu và thực hành các phản ứng hóa học giúp học sinh phát triển tư duy logic và sáng tạo, cùng với sự hiểu biết sâu sắc hơn về thế giới xung quanh.
Hy vọng bài viết này sẽ giúp các bạn học sinh hiểu rõ hơn về các axit quan trọng trong chương trình Hóa học lớp 9, từ đó phát huy khả năng tư duy và chất lượng khi học tập môn Hóa.